|
4 q* S" _' _' N; ~$ A$ x7 h# c1 d 有人曾将接种疫苗的益处与安全饮水比肩。两年多前,面对新冠大流行,疫苗再次以希望的代名词出现。人们对疫苗的期待与认知前所未有地高涨,诸多本土疫苗企业开始走向前台。
0 [; v8 X+ C# g4 Q T 疫情突现时,国内众多科研团队、疫苗企业冲击新冠疫苗研发,数款自研疫苗接连获批。科研成果迭出加之政策绿灯,使这条原本要走8到10年的险途被极大压缩。至今全国超34亿剂新冠疫苗接种的背后,是中国疫苗产业的厚积薄发。 2 L; k8 z! a+ Z) S" {, t- [6 G
 2021年8月2日,市民在南京市鼓楼区五台山体育中心新冠病毒疫苗集中接种点接种疫苗。新华社 图 2021年8月2日,市民在南京市鼓楼区五台山体育中心新冠病毒疫苗集中接种点接种疫苗。新华社 图 十年来,我国疫苗产业市场化程度日益提高。2020年,我国共有334款国产疫苗批件,分属于53家疫苗企业。研发火热与市场繁荣互为催化,近年来,HPV疫苗、流感疫苗、肺炎疫苗、狂犬疫苗——更多拥有自主知识产权的创新疫苗正在加速面市。 & q1 y5 `( Z" J
与此同时,国家免疫规划始终保障有力——国家“买单”的免疫规划疫苗可预防的传染病已达15种,中央财政投入每年已超过40亿。而今,我国多种疫苗可预防传染病已经降到了历史最低水平。
6 {+ N, \9 F2 T; n' c0 r% k 新冠疫苗竞速:短期催化,厚积薄发 : F) Q2 B9 o7 @5 L) C0 k v- A
8月5日,民营疫苗龙头企业重庆智飞生物制品股份有限公司(以下简称“智飞生物”)发布公告称,其全资子公司安徽智飞龙科马生物制药有限公司(以下简称“智飞龙科马”)于近日获得国家知识产权局颁发的一项发明专利证书,该专利名称为“一种CHO细胞表达的重组新型冠状病毒NCP-RBD蛋白的制备方法及其应用”。 / h" i& G7 P' {, A" I$ J" K8 W# W
智飞生物向澎湃新闻介绍,该专利已用于制备其自主研发的重组新型冠状病毒蛋白疫苗(CHO细胞)(以下简称“重组蛋白疫苗”)。 . u# W2 w1 P# s7 d w, I& `1 I- I o
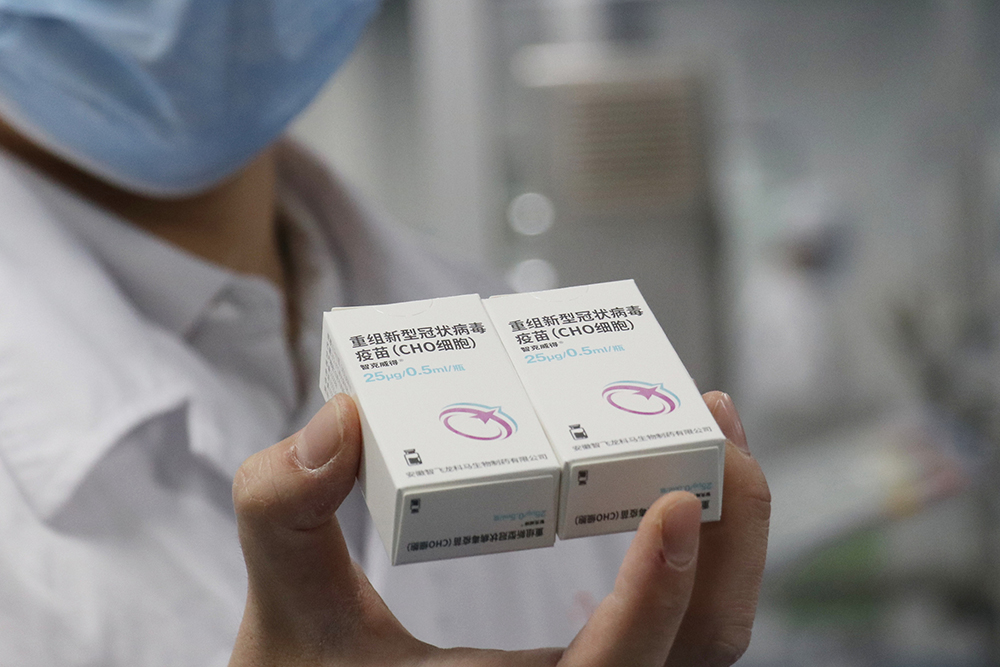 智飞重组新型冠状病毒蛋白疫苗(CHO细胞)。视觉中国 图 智飞重组新型冠状病毒蛋白疫苗(CHO细胞)。视觉中国 图 2021年3月,在疫情正吃劲时,这款重组蛋白疫苗被纳入紧急使用,成为当时国内第四款获批紧急使用的新冠病毒疫苗,也是全球首个获批紧急使用的新冠重组蛋白疫苗。2022年3月1日,该疫苗获批附条件上市。同期,该疫苗被纳入“加强针”进行序贯接种。
' k2 h4 R7 f& V1 X/ H6 z 智飞生物2021年年报披露,报告期内,这款重组蛋白疫苗已为超1亿民众提供保护。 : u: H/ q+ u& A, b2 }8 r6 K
该疫苗为智飞生物与中科院微生物所高福、严景华团队合作研发。近日,智飞生物党委书记、董事长、总裁蒋仁生在接受澎湃新闻采访时介绍,“微生物所做的是最上游,RBD(受体结合结构域)二聚体这块用了他们的专利,后续的工艺则是我们负责的。” / j3 r0 p* @: `2 ?6 D
今年5月4日,国际顶级医学学术期刊《新英格兰医学杂志》在线发表了该疫苗的Ⅲ期临床试验结果,临床结果显示,受试者(≥18岁)在完成全程接种后,该疫苗预防任何严重程度新冠肺炎的保护效力达81.4%(95% CI, 73.3~87.3);在全程接种后6个月的长期有效性分析中,有效性的幅度下降较小,但预防任何严重程度新冠肺炎的保护效力仍然可达75.7%(95% CI,71.0~79.8)。 ! f& Z0 Y% H* L8 Z; z
“这个数据令人鼓舞,国产新冠疫苗也能与全球研发的新冠疫苗在安全性和有效性上竞争。”蒋仁生表示。 1 `) K7 D! M3 w/ @. h
为了应对病毒的快速变异,这款重组蛋白疫苗的“更新”研究正在进行中。蒋仁生介绍, “新一代”的重组蛋白疫苗有望成为可同时预防奥密克戎和德尔塔变异株的“二价疫苗”。 9 D V) U3 I( ^+ w. ?) e
今年4月26日(当地时间),国际顶级学术期刊《细胞》报道了这款“新一代”疫苗的研究进展,作者为智飞生物的合作方高福院士团队及其他合作团队。研究者们开发了针对新冠流行变异株的嵌合RBD二聚体蛋白疫苗的设计方法,其为两个异源的RBD串联形成。 # R$ Y' `8 K" S m3 ?8 ]
研究者们设计了Delta-Omicron嵌合蛋白疫苗,与prototype(原型毒株)同源RBD二聚体疫苗相比,其免疫小鼠刺激产生更加广谱的抗体反应,对Delta和Omicron变异株的攻毒均表现出更好的保护效果。研究者表示,这些研究数据支持开发适应变异株的多价疫苗以预防流行变异株。
# Q* Y- V% @( o: ]( ]2 m! U 今年5月,高福在一场公开访谈中讲到,团队不但在设计针对两种变异株的二聚体疫苗,还在设计针对三种变异株的三聚体疫苗。高福介绍,这种设计的好处在于,“发射塔不变”,未来再出现新的变异株,“可以随时更换弹头”。
+ t* n& [+ ^; Y% J. P 奥密克戎变异株的出现和快速流行让原本白热化的疫苗研发竞速再开一局。
& e% l; ]' l. B8 D O! s# @ 今年4月下旬以来,中国生物及科兴开发的奥密克戎株灭活疫苗均已进入临床试验阶段。中国生物首席科学家、副总裁张云涛曾在今年5月介绍,针对奥密克戎变异株,中生不光布局了灭活疫苗,重组、mRNA的技术路线也在同步进行。
& V+ R. Z& d1 P5 z6 n B0 {% z  2022年8月29日,北京,中国国际服务贸易交易会上,国药集团新型冠状病毒mRNA疫苗。视觉中国 图 2022年8月29日,北京,中国国际服务贸易交易会上,国药集团新型冠状病毒mRNA疫苗。视觉中国 图 新的竞速仿佛疫情初现时的重演,不过一切显得更为迅疾有序。 # h- s) l6 O) W* U1 K) b
2020年疫情初期,我国疫苗研发在灭活疫苗、腺病毒载体疫苗、重组蛋白疫苗、核酸疫苗(mRNA疫苗及DNA疫苗)、减毒流感病毒载体疫苗这5条技术路线上同步推进。据新华社2022年10月12日消息,目前,我国已有46款新冠病毒疫苗进入临床试验,21款在境外获批开展Ⅲ期临床试验,灭活疫苗、腺病毒载体疫苗、重组蛋白疫苗等9款疫苗获批附条件上市或紧急使用,3款疫苗纳入世界卫生组织紧急使用清单。
, d& u: o7 I3 J' N7 P+ i1 _ 同时,我国新型新冠病毒疫苗研发取得新进展。我国有3款奥密克戎变异株单价灭活疫苗正在中国内地、香港以及阿联酋开展序贯临床试验,目前试验进展顺利。已有9款涉及变异株的多价疫苗进入临床试验阶段,其中一些正在开展Ⅲ期临床试验。同时,我国正在积极部署推进广谱疫苗的研发工作。 * j+ p- J' v4 O# h. }' O* M$ v
新冠疫情就像国内疫苗产业发展的“催化剂”,一时喷薄而出。
3 T5 Z5 d8 C7 ?9 Q$ h HPV疫苗热潮:进口香,国产旺
: n* X" L7 J+ |1 C4 J 在新冠疫苗之前,另一款全民热议的疫苗是HPV(Human Papilloma virus,人乳头瘤病毒)疫苗。一方面是需求爆棚,一方面是供应紧张,“HPV疫苗一针难求”的话题不断刷屏。
" d5 z, N; Z# I; t% ^: U& v7 [/ Y 目前,我国已有5款HPV疫苗获批注册,其中2款是国产疫苗,3款是进口疫苗。2款国产疫苗分别为今年3月获批的沃森生物旗下的二价HPV疫苗和2019年12月获批的万泰生物旗下的二价HPV疫苗。3款进口疫苗分别是葛兰素史克(GSK)的二价苗、默沙东的四价苗和九价苗。 0 q% T: v7 T# ]: ]# S9 k
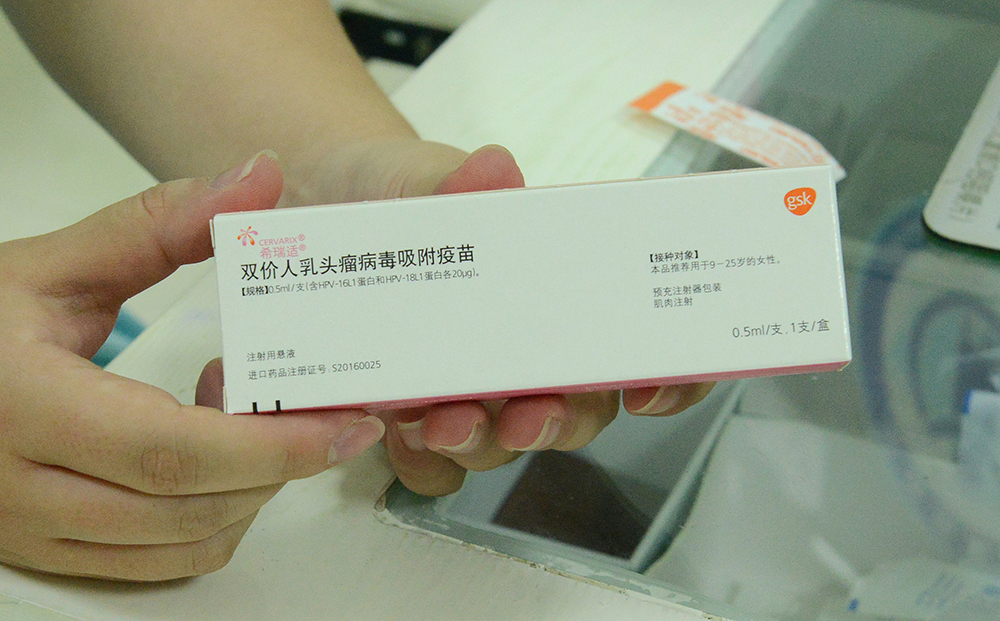 医务人员展示葛兰素史克(GSK)的二价HPV疫苗 视觉中国 图 医务人员展示葛兰素史克(GSK)的二价HPV疫苗 视觉中国 图 HPV疫苗价数越高预防的HPV型别越多。不过即便接种二价苗也有良好获益——二价苗可预防的两种HPV型别是16型、18型,流行病学研究显示,HPV16和HPV18型是宫颈癌中最常见的高危型HPV型别,在中国,约84.5%的宫颈鳞癌病例都与这两个高危型HPV感染有关。
0 [ [& p$ Z! ^. f0 c6 H& y 宫颈癌是严重威胁全球女性健康的常见恶性肿瘤。IARC(世界卫生组织国际癌症研究机构)数据显示,2020年全球范围内宫颈癌新发60万例,死亡34万例;其中,中国新发宫颈癌11万例,死亡6万例,每年新发死亡病例约占全球的20%。 - h0 `2 U4 i) p6 o
宫颈癌也是目前医学界唯一明确病因的癌症,持续性的高危HPV病毒感染被认为是宫颈癌的重要病因。HPV疫苗则是全球首个把癌症作为适应症列入说明书的疫苗。 / S* ]) |& U% C4 C6 P, q0 L. {
在今年5月30日召开的国家卫健委新闻发布会上,中华预防医学会妇女保健分会主任委员、中国疾控中心慢性病首席专家王临虹介绍,国家常规疫苗报表数据显示,2018年至2020年,我国HPV疫苗接种数量在逐年上升,从2018年的341.7万上升至2020年的1227.9万剂次。但整体上看,目前HPV疫苗仍处于供不应求的状态,适龄女性HPV疫苗接种率仍处于较低水平。
( \- g0 y; x+ u/ i5 U  市民接种HPV疫苗 视觉中国 图 市民接种HPV疫苗 视觉中国 图 面对巨大的需求缺口,近年来众多国内疫苗企业竞速研发。就已上市的两款二价HPV疫苗的研发上市历程来看,均经历了近10年甚至更长时间。
1 C0 a& P7 A8 C 万泰生物曾在2021年11月在投资者互动平台表示,二价HPV疫苗项目从2003年启动,2017年11月完成三期临床申报上市,2019年12月30日获批上市,2020年5月正式投入市场。照此计算,从启动到上市中间历经约17年时间。 2 K: X/ u9 {9 Y
此外,沃森生物控股子公司泽润生物技术有限公司的二价HPV疫苗早在2011年6月就获得了药物临床试验批件,2020年6月申请新药上市许可获得《受理通知书》,前后历时约9年。
# U9 _0 z2 Y* P0 R' S 除了已上市HPV疫苗外,国内多款在研疫苗正紧锣密鼓的推进临床试验。
& P8 V4 v6 r* i 对于二价HPV疫苗,除了已上市的GSK、万泰生物、沃森生物产品外,瑞科生物也在此布局。而成都生物制品研究所、唯博生物、上海生物制品所等正紧锣密鼓地进行四价疫苗的临床试验。对于九价疫苗,除了获批上市的默沙东九价苗,万泰生物、瑞科生物、康乐卫士的九价疫苗均进入Ⅲ期临床阶段。
9 w% a" ]1 n9 u0 s9 C 更多创新疫苗的研发也在同步发力。 % y1 L5 t& p0 N8 O8 h
目前,中国生物研究院和成都生物制品研究所合作的11价HPV疫苗已启动Ⅲ期临床试验,神州细胞与北京诺宁生物联合研发的十四价HPV疫苗已进入II期临床试验。今年3月,成大生物与康乐卫士合作研发的十五价HPV疫苗获批临床,这是当时全球范围内获准开展临床试验的最高价型HPV疫苗。 8 _3 K( |' n/ Q1 K: P
在业内人士看来,随着HPV疫苗国产替代加速,市场供给有望迅速提升。 9 U) h" M7 u1 v# {3 I4 |7 _
同时,在政策层面,我国HPV疫苗免费接种地区正不断扩围,疫苗可及性进一步提升。 & j6 W' X$ [5 \; b1 G: @* }
今年7月,国家卫健委介绍,目前我国HPV疫苗接种未纳入国家免疫规划,按照自费自愿的原则接种。广东、海南、福建3省已先后启动实施全省适龄女孩免费接种国产二价HPV疫苗工作,并纳入2022年省委、省政府为民办实事项目。
: `. ?9 d% l6 @6 z 国家卫健委表示,将大力推广广东、海南、福建等省份经验,总结各地利用政府民生项目和医保基金等多渠道筹资的经验做法,鼓励地方先行先试,重点推动条件成熟的地区率先出台免费HPV疫苗接种政策,不断提高适龄女孩HPV疫苗接种率。
# n7 I% a9 y# D: E: |3 \6 P 二类疫苗“战场”:自主研发,坚持创新 + V1 J( Z; Z& q A1 M+ `
在我国,疫苗分为一类疫苗、二类疫苗两类。其中,一类疫苗为国家免疫规划疫苗,由政府采购免费向公民提供,二类疫苗则由公民自费自愿接种。 0 v7 ^" y% c$ I5 I3 w. Q* u
我国是世界上为数不多的能够依靠自身力量解决全部免疫规划疫苗的国家之一。目前我国国家免疫规划疫苗可预防的传染病已达15种,主要覆盖0-6岁儿童。 " E$ L, ~& \4 k9 w7 g- K
从供给侧来看,一类疫苗利润较低,主要由中国医药集团有限公司(简称“国药集团”)旗下的中国生物技术股份有限公司(简称“中国生物”)提供,相较而言,遵循市场导向的二类疫苗才是广大疫苗民企角逐的主赛场,上文所述的HPV疫苗即是鲜明一例。
; g1 m: B* x5 v- d. K  视觉中国 图 视觉中国 图 近年来,众多本土企业正发力流感疫苗、肺炎疫苗、狂犬疫苗、流脑类(流行性脑脊髓膜炎)疫苗等大品种二类疫苗的自主研发。 0 s7 _& V$ q F$ V8 Q, X
2019年,中国疫苗产业迎来了历史性的重磅变革——当年12月1日,《中华人民共和国疫苗管理法》正式施行。这是全球首部综合性疫苗管理法律,充分体现了党中央对疫苗的高度重视,对促进疫苗产业创新和行业健康发展具有重要意义。 ( O- d6 H. E) [( q- `: g
《疫苗管理法》明确,国家鼓励疫苗上市许可持有人加大研制和创新资金投入,优化生产工艺,提升质量控制水平,推动疫苗技术进步;支持多联多价等新型疫苗的研制。
4 N+ B. y- S+ d9 h 彼时,我国共有45家疫苗生产企业,可生产60种以上疫苗,预防34种传染病,年产能超过10亿剂次,国产疫苗占实际接种量的95%以上。但研发创新能力不强,仍制约着我国疫苗产业进一步做强做优做大。 , b! o1 e; ]; J: I3 Y, T8 k
研发力量、创新能力,越来越成为市场对一家疫苗企业的终极之问。这对于智飞生物来说也是一个亟需回答的问题。2019年,其代理产品在总营收中的占比为87.37%;到2020年,这个数字进一步上升为92.09%,相较而言,其自主研发产品在总营收中的占比还不到一成,这引发了市场的诸多议论。 : ]) I) _& L* l, z. ?( `, z- M3 M: P
而到了2021年,这一局面明显改观。智飞自主研发产品的营收占比显著提升至31.64%。公司业绩也实现了突破,当年营收306.52亿元,较上年同期增长101.79%。
7 ~& Q8 {; B2 W 对于业绩驱动因素,公司2021年报分析的第一点即为“自主研发,坚持创新”。2021年,其不但有自研的重组新型冠状病毒蛋白疫苗(CHO细胞)被纳入紧急使用,公司自主产品注射用母牛分枝杆菌(微卡)也于2021年6月获批增加适应症,新增预防结核分枝杆菌潜伏感染人群发生肺结核疾病。 ) S3 t7 D7 K a% r( L# Q
微卡是智飞生物全资子公司安徽智飞龙科马的自主产品。近两年,智飞龙科马作为重组蛋白疫苗的研发公司而声名鹊起。事实上,在2008年被蒋仁生收购时,龙科马的使命并不是研发病毒类疫苗,而是做结核防控产品。 / [* X5 u1 y7 d. p4 ]! D% @/ k
 智飞生物的自主产品:注射用母牛分枝杆菌(微卡) 智飞生物官网 图 智飞生物的自主产品:注射用母牛分枝杆菌(微卡) 智飞生物官网 图 结核俗称痨病。过去,我国民间有“十痨九死”的说法。建国前,结核一度广泛流行,甚至成为一种文化现象。鲁迅的小说《药》中,华老栓夫妇为儿子买人血馒头,就是为了治痨病。鲁迅本人也死于肺痨。 9 U' N s$ ^4 C: C
作为一种消耗性疾病,肺结核会让人逐渐丧失劳动能力,而又要长期用药。所以老百姓还有“致富十年功,痨病一场空”的说法。 - ]. N& Z* a+ E, f. O1 X
2002年辞职创立智飞生物前,蒋仁生曾在基层疾控系统工作过25年,最初的十几年就在老家广西壮族自治区桂林市灌阳县防疫站,“当时村村寨寨我都跑遍了,138个生产大队、300多个村医我都熟悉。”当时他负责过结核防治工作,他清楚地记得,不少家庭的主要劳动力都感染了结核病,无法从事重体力劳动,又得花钱治病,造成全家生计窘迫。 # ~: M' u, d& @: s6 c" L! @! K
目前,我国结核防控形势仍不容乐观。世卫组织发布的《2021年全球结核病报告》显示,2020年,我国估算的结核病新发患者数为84.2万,发病率约为59/10万。结核病新发病例总数排全球第2位,仅低于印度(259万)。 4 y3 M, p, V, N! v
据人民日报健康客户端今年3月消息,中国医学科学院病原生物学研究所研究员高磊介绍,“我国(结核)潜伏感染者数量是非常巨大的,流行病学调查发现,5周岁以上的全国人口,大概有18.1%的人潜伏感染状态,15岁以上的成年人,潜伏感染率大概是20.3%”。中国疾控制中心结控中心主任赵雁林表示,对这部分潜伏感染人群的预防性干预至关重要。 $ r" n4 f( ?5 |& G$ R
江苏省疾控中心慢性传染病防治所副所长竺丽梅介绍,“化学药物预防治疗常用药物包括一线抗结核药物异烟肼、利福平、利福喷丁,免疫预防治疗是我国自主研发的注射用母牛分枝杆菌‘微卡’,如今已获国家药品注册证书,WHO在‘结核病研究与发展战略规划’中予以推荐”,“该产品的批准上市,为结核潜伏感染者预防性治疗提供了新的方法,有利于控制结核病疫情。”
u7 Z$ |7 S& b) ]1 B 从2008年龙科马被收购,到2021年“微卡”获批新增预防适应症,这款结核防治产品的研发经历14年。 2 h0 v) m+ h+ p$ e5 h& r1 `
中国疫苗启航:砥砺前行,走向超越
- a0 H/ P9 q. M2 o 对于生物制品行业的研发风险,业内有句行话:“十年、十亿美元、10%的成功率”。所以疫苗研发更像是一个赌局。 0 g9 h% j6 h9 K u. C
风险这么大,最初谁来干?当然是“国家队”。
6 @) w1 B: z/ Y' b 我国六大生物制品研究所的格局形成于上世纪50年代,包括北京、长春、兰州、成都、上海、武汉等六个生物制品研究所,早期的麻疹疫苗、A群流脑莱膜多糖疫苗等都是出自这几大所。此外,同样举足轻重的还有中国医学科学院医学生物学研究所,该所建于1958年,预防脊髓灰质炎(小儿麻痹)的糖丸即出自该所。
" z; X2 _8 A( {4 G0 g$ Q7 X& C 曾经,“国家队”为建国后遏制脊灰、天花、流脑(流行性脑脊髓膜炎)等恶性传染病的流行做出了巨大贡献。 # m( K% l0 S. p% U& r- [9 d4 L
蒋仁生辞职创业后的“第一桶金”,即来自于代理了“国家队”的自研疫苗——兰州生物制品研究所研制的A+C群脑膜炎球菌多糖疫苗。
: N* V, j4 \: q/ q 2002年,这款疫苗在国内首家上市,获得当年甘肃省科技进步一等奖。智飞生物在国内C群流脑爆发前率先代理了该疫苗,并在2003年底到2004年初国内多地C群流脑爆发时将其推向市场。智飞生物的疫苗代理业务也从此起步。 ) D! w$ E3 X w; C. _" z
最初,兰州所等生研所既是一个科研生产单位,又是一个履行部分政府职能的事业单位。直到1989年实行政企分开,原六大生研所整合组成中国生物制品总公司,后经更名、重组,于2011年10月改制为中国生物技术股份有限公司,简称“中国生物”。
6 p' S# s* ]2 K2 F. B1 Q 作为生物医药“国家队”,目前,中国生物生产供应着80%以上国家免疫规划用疫苗。 : A1 Z8 s; a# X8 r/ r N/ r
也是从上世纪80年代起,大批民营生物制品企业加入到市场竞争中,并在改革开放的浪潮中逐渐发展壮大。
L9 w# t& s2 R. C6 S 近十年来,我国疫苗产业市场化程度日益提高。2020年,我国共有334款国产疫苗批件,分属于53家疫苗企业,其中中国生物下属六大所占比55.7%。 * ^1 @$ d6 v2 M3 h x7 u
2020年,直面新冠疫情,一批本土疫苗企业迎来“大练兵”。
, Z9 z1 n/ I" D8 ~1 o 西北大学公共管理学院副教授徐娟在《产业蓝皮书:中国产业竞争力报告(2021)》中写道,中国新冠疫苗是一个里程碑式的产品,其间积累的研发、临床和商业化经验将帮助一批优秀中国本土企业迅速成长起来。在新冠疫苗研发中,以国药中生、科兴中维、康希诺、智飞生物、康泰生物、沃森生物/艾博生物为代表的一批中国疫苗企业飞速成长。
. f; u0 V9 G2 a5 Z9 @# w9 z# j; j  2021年6月1日,北京科兴中维生物技术有限公司的疫苗包装生产线。视觉中国 图 2021年6月1日,北京科兴中维生物技术有限公司的疫苗包装生产线。视觉中国 图 徐娟同时对比了中国本土与欧美发达国家疫苗产业的差异:疫苗产业以大品种驱动的特点十分明显。2020年全球销量前十的重磅疫苗均为四家跨国疫苗公司生产,排名第一的是辉瑞的13价肺炎疫苗,仅此一款疫苗销售额就达58.5亿美元,约合当年中国疫苗市场的总规模(364亿人民币)。 s' B [* t$ i6 }. i8 j
“未来中国是否能够诞生世界级的疫苗企业,新冠疫苗为中国疫苗行业提供了前所未有的发展契机。”徐娟写道。
; d2 L: M# I* b8 W- Q5 U, j. R 据新华社10月12日消息,近日,我国又有一款吸入用腺病毒载体疫苗和一款重组蛋白疫苗获批,可在完成两剂灭活疫苗接种后六个月在规定人群中开展序贯加强免疫紧急使用。其中,重组新型冠状病毒融合蛋白疫苗Ⅲ期临床试验关键数据分析结果显示,在两针灭活疫苗的基础上采用该重组蛋白疫苗进行序贯加强免疫,对于奥密克戎变异株感染引起的新冠肺炎(轻型及以上)可产生良好的保护力,并具有良好的安全性。 9 U$ m/ z9 ^8 r7 q- c
# o/ N/ ~4 }% _ a5 g
2021年11月12日,第五届海南国际健康产业博览会在海南省海口市开幕。康希诺携全球首款吸入式腺病毒载体新冠疫苗克威莎亮相,一位记者用纯净水体验仿雾化吸入式疫苗接种过程。 中新社记者骆云飞/视觉中国 图 & n: ]. d! v2 s$ k, j
这款重组新型冠状病毒融合蛋白疫苗为“珠海造”,拥有自主知识产权。据珠海市委宣传部官方微信公号“珠海发布”消息,这款疫苗由珠海丽珠医药集团旗下的丽珠单抗生物有限公司与中国科学院生物物理研究所合作研发,历时两年零39天,目前丽珠医药集团已建成了新冠疫苗原液年产能达35亿剂、制剂年产能达15亿剂的生产车间。
& S4 `! \0 L4 ] 在蒋仁生看来,现在整个行业都在努力,“国家的政策也越来越好,我们总会逐渐赶超的。” # T" A5 J4 J! o" ]
今年5月10日,《“十四五”生物经济发展规划》正式出台,这是我国首部生物经济五年规划。规划提出,重点围绕药品、疫苗、先进诊疗技术和装备等方向,提升原始创新能力,加强药品监管科学研究,增强生物医药高端产品及设备供应链保障水平,有力支撑疾病防控救治和应对人口老龄化。
: m5 L/ x0 E! h2 B6 g) o4 W 当前,我国政府免费向居民提供的国家免疫规划疫苗可预防的传染病已达15种,中央财政投入每年已超过40亿,目前我国多种疫苗可预防传染病已经降到了历史最低水平。同时,更多拥有自主知识产权的创新疫苗正在加速面市。 ! N9 H5 i2 `/ C( K) u" @0 F
一剂疫苗正为健康中国蓝图注入强大信心。 7 I: Z6 [/ V7 F, @3 [& c6 V
% N% P5 \& N4 k7 U6 U
" R$ {) j; F$ z; I' B0 q: [. }
" s/ P! ?6 c$ Y! b6 C8 a
( H$ M3 |* H- }9 }" j. I, R, n5 b1 o6 Y H' r B, m
. a. ]* t4 O6 J
+ Z1 @" v5 u" Z' o% D, H! B2 ^6 ~ B0 C. K
; D( z( `& W, |0 y+ Y) C4 M
2 N$ D9 F" `% i$ [3 h* n# I
# F$ K! U3 K; w7 B0 E9 E | 

